قوة الأحماض
تكمن قوة الحمض في ميله إلى التخلي عن H
+
(بروتون) في الماء، يتم تحديده في شكل ثابت توازن معين، K
a
يمكن للحمض أن يتخلى عن بروتونه بسهولة أكثر أو أقل وفقاً إذ أنه أكثر أو أقل قوة و
إذا كان الحمض قويًا جدًا فإنه يتخلى عن البروتون بسهولة وستكون قاعدته المقترنة ضعيفة جدًا.
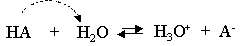
الأحماض المعدنية Mineral acids
هو الحمض المشتق من المعادن الغير عضوية (Inorganic mineral) عن طريق التفاعلات الكيميائية.
- تكمن وظيفة الأحماض المعدنية في أستخدامها كعوامل حفازة وعوامل مساعدة في التفاعلات الكيميائية، وكذلك تستخدم كعوامل منظفة بصناعة الإلكترونيات.
- الأحماض المعدنية يميزها سهولة الذوبان في الماء، حيث أنها متأينة في الماء (مركبات قطبية)، فلها شحنات سالبة وشحنات موجبة.
- أغلبيتها أحماض قوية ولكن هناك أحماض معدنية ضعيفة مثل حمض الفوسفوريك.
- الأحماض المعدنية أغلبها لونها شفاف ورائق، وعندما يتعكر لونها هذا ذليل على وجود بعض الشوائب والغازات.
- سهولة تحرير الحمض العضوي للبروتون مرتبطة بقوة أو ضعف الحمض.
- يسهل إيجاد العلاقة بين ثابت قوة الحمض وثابت قوة الأساس لزوج (حمض، أساس مرافق) في الماء.[1]
أمثلة عن الأحماض المعدنية
- حمض الهيدروكلوريك
-
حمض النيتريك: HNO
3
-
حامض الفوسفوريك: H
3
PO
4
-
حامض الكبريتيك : H
2
SO
4
-
حمض البوريك : H
3
BO
3
-
حمض الهيدروفلوريك
: HF - حمض الهيدروبروميك: HBr
-
حمض البيركلوريك: حمض الهيدروكلوريك
4
- حمض الهيدرويوديك
ترتيب الأحماض المعدنية
في الجدول الموضح أدناه، ترتبت الأحماض وقفاً لتناقص قوتها (وهى مقدرتها على منح (H
+
)، وبفحص الحمض (HClO
4
) نجد أنه الأقوى حمضية وقاعدته القرينة (ClO
4
–
) تكون الأضعف قاعدية بمعني أن العلاقة بين الحمض وقاعدته القرينة علاقة عكسية.

لماذا سميت الأحماض المعدنية بهذا الأسم رغم عدم احتوائها على معادن
هناك أختلاف بين كلمة (Mineral) وبين كلمة (Metal)
: كلمة (Metals) هي المعادن العادية المعروفة في الجدول الدوري، أما كلمة (Mineral) تشير لمواد صلبة غير عضوية، تتكون بشكل طبيعي دون أي تدخل أنساني وتتوفر العثور عليها في قشرة الأرض. وتكوينها الكيميائي واضح ولها هيكل بلوري.
أصل الأحماض المعدنية أملاح معدنية، فحمض الهيدروكلوريك من ملح الطعام، والكبريتيك من الكبريت
وحمض الكبريتوز
هو الحمض الأكسجيني من الكبريت، والفوسفوريك من الفوسفور والنيتريك من النترات وهكذا، وكل حمض من له حكاية وقصة من حيث مصدره وتكوينه.
ما هو الحمض القوي
- هو الحمض الذي إذا تأين تماماً أصبح قادر على إعطاء أكبر عدد من أيونات H + أو بروتونات وقت خلطها في محلول، هذه الأيونات هي الجسيمات المشحونة، فهذا يعني أن الحمض القوي هو الحمض الموصل للكهرباء.
-
يمكن أن تبجيل هذه التفاعلات الكيميائية، ولكن يحدث هذا في حالات قليلة، وقتها يتخلص من الحمض H
+
من أيون بسهولة، ويتم فصل الحمض بالكامل. -
توضيح بمثال: إذا ذاب كلوريد الهيدروجين في H
2
O لكى يصنع حمض الهيدروكلوريك، يحدث القليل من التفاعل العكسي، وفي وقت واحد، يمكن أن يحدث تفاعلاً افتراضياً مائة بالمائة حيث يظهر كلوريد الهيدروجين في تفاعل مع H3O
+
(أيون الهيدروكسونيوم) و(Cl
–
أيونات)، في تلك الحالة يكون الحمض القوي هو كلوريد الهيدروجين.
-
ولا يمكن ذكر الأحماض القوية دون ذّكر
اقوى حمض في العالم
هو
حمض
الفلوروانتيمونيك، و الحمض الفائق وتعريفه التقليدي هو حمض لديه حامضية أعلى من حمض الكبريت،
وحمض الكاربورين
(Carborane Acid) حمض الفحم، وهو أول حمض فائق يمكن حفظه في وعاء.
أمثلة على الأحماض المعدنية القوية
الأحماض القوية أيوناتها تتفكك تماماً في الماء، مما ينتج عنه تولد بروتون واحد أو أكثر (كاتيونات الهيدروجين) لكل جزيء، ويوجد 7 من الأحماض القوية المشتركة في ذلك:
- حمض الهيدروكلوريك
- HI – حامض هيدرويدي
- HBr – حمض الهيدروبروميك
-
HClO
4
– حمض البيركلوريك -
H
2
SO
4
– حامض الكبريتيك -
HClO
3
– حمض الكلوريك -
HNO
3
– حمض النيتريك
ما هو الحمض الضعيف
هو أقل قدرة في إعطاء البروتونات مقارنة بالحمض القوي.حيث يؤكد الكيميائيون أن الحمض ضعيف هو الحمض الذي إذا تأين نتج تأين جزئي أو غير كامل، وبالتالي ينتج عن هذا التأين إطلاق لبعض ذرات الهيدروجين فقط في المحلول. وبالتالي، تحتوي الأحماض الضعيفة على pKa أعلى من الأحماض القوية.
أمثلة على الأحماض المعدنية الضعيفة
من الأمثلة الجيدة على حمض ضعيف هو حمض إيثانويك، الذي يظهر تفاعل مع H
2
O فينتج عن التفاعل H3O
+
(أيونات الهيدروكسونيوم) و CH
3
COOH (أيونات الإيثانوات)، ولكن ما يميز هذا التفاعل هو التفاعل العكسي الذي يُظهر نجاحاً أكبر من التفاعل الأمامي. حيث تتفاعل الجزيئات بسهولة تامة لتحسين الحمض.
- حمض الفوسفوريك
-
حمض الخليك (CH
3
COOH) - حامض الكبريتيك
- حمض الهيدروفلوريك (HF)
- حمض الفورميك (HCOOH)
-
حمض النيتروز (HNO)
2
) - حمض البنزويك
الفرق بين الحمض القوي والحمض الضعيف
| الحمض القوي | الحمض الضعيف | |
| التوصيل الكهربي | تكون الأحماض القوية دائمًا موصلية قوية للتيار الكهربي. عادة ما تمر الأحماض القوية تيارًا أكبر مقارنة بالأحماض الضعيفة لنفس الجهد والتركيز | تكون الأحماض الضعيفة لها مقدرة منخفضة على توصيل التيار الكهربي. ويطلق عليهم الموصلات الفقيرة. |
| الرقم الهيدروجيني | يكون الرقم الهيدروجيني أقل، بشكل عام 3. ويكون تركيز الأحماض القوية من أيونات H + عالي (الحمض الذي يحتوي على الرقم الهيدروجيني 3 يحتوي على 0.001 مول لكل لتر من أيونات الهيدروجين) | يحتوي الحمض الضعيف على درجة حموضة تتراوح بين 3-7. |
| نسبة التفاعل | يكون للحمض القوي قدرة على التفاعل بمعدل أسرع | يكون للحمض الضعيف معدل أبطأ في التفاعل |
| قيمة pKa | تكون قيمة pKa منخفضة كثيراً في الحمض القوي، . | تكون قيمة pKa عالية كثيراً في الحمض الضعيف. |
تأين الأحماض الضعيفة
يعتبر الكيميائيون أن سهم التفاعل لتأين الحمض القوي في الماء سهمًا بسيطًا من اليسار إلى اليمين. وعلى عكس ذلك بالنسبة لحامض ضعيف تجد إن سهم التفاعل متأين في الماء هو سهم مزدوج، مما يدل على أنه عند التوازن يحدث كلا من التفاعل الأمامي والعكسي، عندما يكون القاعدة المترافقة والحمض الضعيف وأيون الهيدروجين متوفر في المحلول المائي.
الشكل العام لتفاعل التأين هو:
HA ⇌ H
+
+ A
–
مثال توضيحي: بالنسبة لحمض الأسيتيك، يتخذ التفاعل الكيميائي الشكل التالي:
H
3
COOH ⇌ CH
3
COO
–
+ H
+
القاعدة المترافقة لحمض الأسيتيك هى أسيتات الأسيتات (في الجانب الأيمن/ المنتج).
الفرق بين الأحماض المعدنية والأحماض العضوية
تعرف الأحماض على أنها تلك المركبات الكيميائية التي لها خصائص حمضية. ويمكن تعريف الحمض على أنه نوع كيميائي لديه القدرة على أن يتفاعل مع قاعدة، وينتج عن التفاعل ملح وماء، ويمكن أيضاً أن تصنف الأحماض على أنها أحماض معدنية وأحماض عضوية وذلك يتوقف على التركيب الكيميائي للحمض.
الفرق الأساسي بين الأحماض العضوية والأحماض المعدنية هو أن الأحماض المعدنية عبارة عن مركبات غير عضوية أساس تكونها المجموعات المختلفة من العناصر الكيميائية بينما الأحماض العضوية أساس تكونها المركبات العضوية التي تتكون في الأصل من ذرات كربون والهيدروجين.[2]

التعليقات مغلقة.